Что же такое кристаллы? Как отличить кристаллы от некристаллических жёстких тел? Возможно, по многогранной форме? Но у кристаллических зерен в металле либо в горной породе форма неверная; а иначе, стекло, к примеру, также возможно многогранным — кто не видел граненых стеклянных бус? Но мы говорим, что стекло — некристаллическое вещество. По какой причине?
В первую очередь по причине того, что кристаллы сами, без помощи человека, принимают собственную многогранную форму, а стекло должно быть огранено рукой человека.
Все вещества в мире выстроены из небольших, не видимых глазом, непрерывно движущихся частиц — из ионов, атомов, молекул.

РАЗНЫЕ ФОРМЫ КРИСТАЛЛОВ: 1 — висмут (скелетный рост); 2 — гидроборацит; 3 — дендриты меди; 4 — кристаллы льда на стекле; 5 — гематит; 6 — турмалин; 7—серебро; 8 — арагонит; 9 — аметисты
Главное же различие между стёклами и кристаллами содержится в их внутреннем строении, в том, как находятся в них небольшие частички вещества — молекулы, ионы и атомы. В газообразных телах, жидкостях и некристаллических жёстких телах, к примеру в стекле, небольшие частицы вещества расположены совсем непоследовательно. А в жёстких кристаллических телах частицы расположены как бы верным строем. Они напоминают группу физкультурников в строю, с той, но, отличием, что верные последовательности частиц тянутся не только вправо и влево, вперед и назад, но и вверх и вниз. Помимо этого, частицы не стоят без движений, а непрерывно колеблются, удерживаясь на собственных местах электрическими силами. Расстояния между частицами в кристаллов мелки так же, как мелки и сами атомы: на отрезке длиной в 1 см возможно расположить приблизительно 100 млн. атомов. Это большое число: представьте себе, что 100 млн. человек выстроены в шеренгу плечом к плечу. Такая шеренга имела возможность бы опоясать Почву по экватору.
Верный строй частиц в каждом веществе разен, исходя из этого так многообразны формы кристаллов. Но у всех кристаллов атомы либо молекулы непременно находятся в строгом порядке, а у некристаллических тел для того чтобы порядка нет. Исходя из этого мы и говорим: кристаллы — это жёсткие тела, в которых составляющие их частицы расположены верным строем.
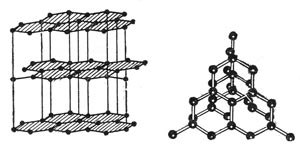
Кристаллические решетки графита (слева) и бриллианта (справа).
Законы построения всех кристаллов теоретически вывели великий русский кристаллограф Евграф Степанович Федоров (1853-1919) и германский кристаллограф Артур Шёнфлис. Превосходно, что Федоров сделал это за 20-летний период перед тем, как в 1912 г. на опыте посредством рентгеновских лучей было доказано, что вправду атомы в кристаллах находятся верным строем и что законы их размещения конкретно таковы, как было гениально предугадано русским ученым.
Верное периодическое размещение атомов (или других частиц) в кристалле именуется кристаллической решеткой.
Любой кристалл имеет собственную характерную многогранную форму, которая зависит от строения его решетки. К примеру, кристаллы поваренной соли имеют в большинстве случаев форму куба, другие вещества кристаллизуются в форме разных пирамид, призм, восьмигранников (октаэдров) и других многогранников.
Но в природе такие верные формы кристаллов видятся редко, об этом вы прочтете дальше.
Некристаллические вещества не имеют собственной формы, в силу того, что составляющие их частицы расположены хаотично, непоследовательно, как говорилось ранее.
Верное размещение частиц определяет и свойства кристалла. Не поразительно ли, к примеру, что два столь разных минерала, как невзрачный тёмный графит и сверкающий прозрачный бриллиант, выстроены из одних и тех же атомов углерода! графит и Алмаз — это кристаллы углерода. В случае, если кристаллические решетки из атомов углерода выстроены по одному примеру, то они образуют прозрачные кристаллы бриллианта, самого жёсткого из всех веществ на Земле и самого дорогого из драгоценных камней. Но в случае, если те же атомы углерода находятся по-второму, то получаются небольшие, тёмные, непрозрачные кристаллы графита — одного из самых мягких минералов. Бриллиант практически в два раза тяжелее графита. Графит проводит электричество, а бриллиант не проводит. Кристаллы бриллианта хрупки, кристаллы графита эластичны. Бриллиант легко сгорает в струе кислорода, а из графита кроме того делается огнеупорная посуда — так он противостоит огню. Два совсем разных вещества, а выстроены из одних и тех же атомов, и отличие между ними только в их разной структуре.

Кристалл бриллианта, отысканный в Якутии (увеличено в 22 раза).
Мы уже заявили, что внутренним строением кристаллов определяются и необычные особенности кристаллов. К примеру, решетка графита состоит как бы из слоев, причем расстояния между этими слоями значительно больше, чем расстояния между отдельными атомами в каждого слоя.
Такие слои относительно легко сдвигаются, скользят один на протяжении другого. Конкретно этим свойством графита мы пользуемся, в то время, когда пишем графитовым карандашом: слои кристаллов графита сдвигаются, и чешуйки графита пристают к бумаге. Лишь, само собой разумеется, любая такая чешуйка представляет собой несколько, а довольно много слоев. Так как расстояние между слоями атомов измеряется стомиллионными долями сантиметра, а приставшие к бумаге чешуйки графита видны несложным глазом.
Строение бриллианта совсем иное, чем у графита; тут нет легко сдвигающихся слоев, и бриллиант выясняется значительно прочнее графита.
Любой знает кристаллы слюды; если вы не видели отдельных кристаллов слюды, то уж возможно встречали блестки слюды в граните либо хотя бы слюдяные пластинки в окнах керосинок. Слюду легко расщепить лезвием ножа либо легко пальцами: листочки слюды отделяются друг от друга практически легко. Но попытайтесь поделить, разрезать либо разбить слюду поперек плоскости пластинки — это весьма тяжело: слюда, непрочная на протяжении плоскости листка, в поперечном направлении выясняется намного прочнее. Прочность кристаллов слюды в различных направлениях разна.
Это свойство опять-таки характерно для кристаллов. Мы знаем, что стекло, к примеру, легко разбивается как угодно, во всех направлениях, на неправильные осколки. А вот кристалл каменной соли, как бы мелко ни разбивать его, постоянно останется кубом, т. е. он все время легко раскалывается лишь по взаимно-перпендикулярным, совсем плоским граням.
Кристалл раскалывается по тем направлениям, где прочность меньше всего. Не у каждого кристалла это выявляется так светло, как у слюды либо каменной соли — к примеру, кварц не раскалывается по ровным плоскостям,— но у всех кристаллов прочность в различных направлениях разна. У каменной соли, к примеру, в одном направлении прочность восьмикратно больше, чем в другом, а у кристаллов цинка — вдесятеро. По этому показателю возможно отличить кристаллы от некристаллов: в некристаллических телах прочность однообразна по всем направлениям, исходя из этого они ни при каких обстоятельствах не раскалываются по ровным плоскостям.

Кристалл исландского шпата
В случае, если нагревать какое-нибудь тело, то оно начнет расширяться. В этот самый момент легко заметить отличие между веществами кристаллическими и некристаллическими: стекло будет расширяться по всем направлениям одинаково, а кристалл — по различным направлениям различно. Кристалл кварца, к примеру, расширяется в продольном направлении в два раза больше, чем в поперечном. Твердость, теплопроводность, электрические и другие свойства кристаллов кроме этого разны по различным направлениям.
Особенный интерес воображают оптические особенности кристаллов. Разглядываемые через кристаллы исландского шпата предметы кажутся удвоенными. В кристалле исландского шпата (и во многих вторых кристаллах) луч света раздваивается. И это свойство также различно по различным направлениям: в случае, если поворачивать кристалл, то буквы будут раздваиваться то больше, то меньше.
По собственной форме кристаллы различных веществ резко отличаются друг от друга. Для кристаллов каменной соли, как вы уже понимаете, обычна форма кубов, для берилла — призма с пирамидами, для бриллианта — восьмигранники с треугольными гранями, так именуемые октаэдры. У каждого вещества имеется собственная характерная форма кристаллов.
Формы кристаллических многогранников поражают взор собственной строгой симметрией. Симметричными мы именуем тела, каковые складываются из однообразных, соразмерных частей. Симметрична, к примеру, бабочка: у нее однообразны правая и левая части туловища; в случае, если бабочка сложит крылья, они совместятся.
В кристаллах симметричны ограничивающие их плоскости-грани, ребра и углы, составляющие вершины кристаллических многогранников.
Симметрия кристаллов — ответственное и характерное их свойство. По форме кристаллов и по их симметрии определяют кристаллическое вещество.