Питание бактерий.
Питание. Под едой бактериальной клетки направляться осознавать усвоения и процесс поглощения энергии и пластического материала в следствии преобразовательных реакций. Типы питания прокариот сложны и разнообразны. Они различаются в зависимости от метода поступления питательных веществ вовнутрь бактериальной клетки, азота и источников углерода, метода получения энергии, природы доноров электронов.
Транспорт питательных веществ вовнутрь клетки может осуществляться 3 механизмами: пассивной диффузией, облегчённой активным транспортом и диффузией.
Пассивная диффузия есть неспецифическим энергозависимым процессом, осуществляемым по градиенту концентрации веществ (вещество из среды с большей собственной концентрацией пассивно, в соответствии с законам осмоса, поступает в среду с меньшей концентрацией). Пассивной диффузией вовнутрь бактериальной клетки поступает ограниченное количество веществ, кое-какие ионы, моносахара. Скорость переноса веществ при пассивной диффузии незначительна и зависит от липофильности и размеров транспортирующихся молекул.
Облегчённая диффузия представляет собой энергонезависимый транспорт веществ по градиенту концентрации при помощи ферментов пермеаз. Пермеазы – это своеобразные мембранные белки, содействующие прохождению веществ через цитоплазматическую мембрану. Пермеаза фиксирует на себе молекулу переносимого вещества, вместе с которым пеодолевает цитоплазматическую мембрану, по окончании чего комплекс «вещество – пермеаза» диссоциирует. Освободившаяся пермеаза употребляется с целью проведения вторых молекул. У прокариотов облегчённой диффузией вовнутрь клетки поступает лишь глицерин. Наряду с этим концентрация внутри клетки глицерина соответствует такой вне клетки. Облегчённая диффузия самый характерна для микроорганизмов-эукариот.
Деятельный транспорт – это энергозависимый перенос веществ вовнутрь клетки против градиента концентрации при помощи своеобразных ферментов. Активным транспортом в бактериальную клетку поступает большинство веществ (ионы, углеводы, аминокислоты, липиды и др.). Деятельный транспорт может осуществляться: (1) без химической модификации переносимого вещества; (2) с химической модификацией.
В первом случае молекула питательного вещества образует комплекс с белком периплазматического пространства, что взаимодействует со своеобразной пермеазой цитоплазматической мембраны. По окончании энергозависимого проникновения через цитоплазматическую мембрану комплекс «субстрат – белок периплазмы – пермеаза» диссоциирует с освобождением молекулы субстрата.
При активном транспорте с химической модификацией переносимого вещества цепь событий включает: (1) фосфорилирование мембранного фермента-2 со стороны цитоплазмы фосфоенолпируватом; (2) связывание на поверхности цитоплазматической мембраны фосфорилированным ферментом-2 молекулы субстрата; (3) энергозависимый транспорт молекулы субстрата в цитоплазму; (4) перенос фосфатной группы на молекулу субстрата; (5) диссоциация комплекса «субстрат – фермент» в цитоплазме. За счёт фосфорилирования молекулы субстрата аккумулируются в цитоплазме клеток и не могут выйти из них.
Классификация бактерий по типу питания.
По методу поступления питательных веществ бактерии подразделяются на голофиты и голозои. Бактерии-голофиты (от греч. holos – полноценный и phyticos – относящийся к растениям) неспособны выделять в вохдух ферменты, расщепляющие субстраты, благодаря чего потребляют питательные вещества только в растворённом, молекулярном виде. Бактерии-голозои (от греч. holos – полноценный и zoikos – относящийся к животным), наоборот, имеют комплекс экзоферментов, каковые снабжают внешнее питание – расщепление субстратов до молекул вне бактериальной клетки. Затем молекулы питательных веществ поступают вовнутрь бактерий-голозоев.
По источнику углерода среди бактерий выделяют гетеротрофы и автотрофы. Автотрофы (от греч. autos – сам, trophe – пища) в качестве источника углерода применяют углекислый газ (СО2), из которого синтезируют все углеродсодержащие вещества. Для гетеротрофов (от греч. geteros – второй и trophe – пища) источником углерода являются разные органические вещества в молекулярной форме (углеводы, многоатомные спирты, аминокислоты, жирные кислоты). Громаднейшая степень гетеротрофности свойственна прокариотам, каковые смогут жить лишь в вторых живых клеток (к примеру, риккетсии и хламидии).
По источнику азота прокариоты подразделяются на 3 группы: 1) азотфиксирующие бактерии (усваивают молекулярный азот из атмосферного воздуха); 2) бактерии, потребляющие неорганический азот из солей аммония, нитритов либо нитратов; 3) бактерии, каковые ассимилируют азот, содержащийся в органических соединениях (аминокислоты, пурины, пиримидины и др.).
По источнику энергии бактерии дробят на фототрофы и хемотрофы. Бактерии-фототрофы, как и растения, способны применять солнечную энергию. Фототрофные прокариоты болезней у человека не вызывают. Бактерии-хемотрофы приобретают энергию при окислительно-восстановительных реакциях.
По природе доноров электронов бактерии-хемотрофы подразделяются на литотрофы (от греч. litos – камень) и органотрофы. У литотрофов (хемолитотрофов) в качестве доноров электронов выступают неорганические вещества (Н2, Н2S, NH3, сера, CO, Fe2+ и др.). Донорами электронов у органотрофов (хемоорганотрофов) являются органические соединения – углеводы, аминокислоты и др.
Большая часть патогенных для человека бактерий владеет хемоорганотрофным (хемогетеротрофным) типом питания; реже видится хемолитотрофный (хемоавтотрофный) тип.
По способности синтезировать органические соединения бактерии-хемотрофы подразделяются на прототрофы, ауксотрофы и гипотрофы. Бактерии-прототрофы синтезируют из солей и глюкозы аммония все нужные органические вещества. Бактерии именуются ауксотрофами, если они неспособны синтезировать какое-либо органическое вещество из указанных соединений. Крайняя степень потери метаболической активности именуется гипотрофией. Гипотрофные бактерии снабжают собственную жизнедеятельность, реорганизуя структуры либо метаболиты хозяина.
Не считая азота и углерода, для полноценной жизнедеятельности бактериям нужны сера, фосфор, ионы металлов. Источниками серы являются аминокислоты (цистеин, метионин), витамины, кофакторы (биотин, липоевая кислота и др.), соли серной кислоты. Источниками фосфора помогают нуклеиновые кислоты, фосфолипиды, фосфаты. В высоких концентрациях бактериям необходимы магний, калий, кальций, железо; в намного меньших – цинк, марганец, натрий, молибден, медь, никель, кобальт.
Факторы роста – это вещества, каковые бактерии самостоятельно синтезировать не смогут, но очень в них нуждаются. В качестве факторов роста смогут выступать аминокислоты, азотистые основания, витамины, жирные кислоты, железопорфирины и другие соединения. Для оптимальных условий жизнедеятельности бактерий факторы роста должны быть добавлены в питательные среды.
Метаболизм, превращение энергии
А) Конструктивный метаболизм.
Необходимой фазой питания бактерий есть усвоение питательных веществ, другими словами включение их в поменянном либо модифицированном виде в синтетические реакции по воспроизведению клеточных структур и компонентов.
Протеиновый обмен у бактерий может протекать в 3 фазы: первичный распад белка, синтез и вторичный распад белка. Первичный распад протеиновых молекул до пептонов реализовывают экзоферменты – экзопротеазы, выделяемые бактериями в вохдух. Вторичный распад происходит под действием эндоферментов (эндопротеаз), каковые имеют все бактерии. Данный процесс протекает в бактериальной клетки и содержится в расщеплении пептидов до составляющих их аминокислот. Последние смогут быть использованы в неизменённом виде либо быть подвергнуты химическим преобразованиям (дезаминирование, декарбоксилирование и др.), из-за которых появляются аммиак, индол, сероводород, кетокислоты, спирт, углекислый газ и др. Обнаружение указанных соединений имеет в бактериологии диагностическое значение.
Наровне с реакциями расщепления белков, происходят реакции их синтеза. Одни бактерии образуют белки из готовых аминокислот, взятых в следствии внешнего питания, другие бактерии самостоятельно синтезируют аминокислоты из несложных соединений, содержащих углерод и азот. Синтез аминокислот может осуществляться в реакциях аминирования, переаминирования, амидирования, карбоксилирования. Большая часть прокариот способны синтезировать все аминокислоты, входящие в состав клеточных белков. Изюминкой синтеза аминокислот есть применение неспециализированных биосинтетических дорог: цикл трикарбоновых кислот, гликолиз, окислительный пентозо-фосфатный путь и др. Главным исходным соединением для синтеза аминокислот есть пируват и фумарат.
Углеводный обмен у гетеротрофов и автотрофов имеет отличия (схема 1). Бактерии-автотрофы все нужные углеводы синтезируют из углекислого газа. Сырьём для образования углеводов у бактерий-гетеротрофов могут служить: (1) одно-, двух- и трёхуглеродные соединения; и (2) полисахариды (крахмал, гликоген, целлюлоза). Для расщепления последних многие бактерии-гетеротрофы имеют экзоферменты (амилаза, направляться и др.), каковые выполняют гидролиз полисахаридов до образования глюкозы, мальтозы, фруктозы и пр.
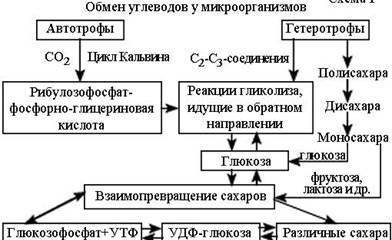 |
У бактерий-автотрофов в цикле Кальвина из углекислого газа образуется рибулозофосфат-фосфорно-глицериновая кислота, которая включается в реакции гликолиза, идущие в обратном направлении. Конечным продуктом обратного синтеза есть глюкоза.
Бактерии-гетеротрофы образуют глюкозу из одно-, двух- и трёхуглеродных соединений, кроме этого включая их в реакции обратного гликолиза. Ввиду того, что кое-какие реакции гликолиза необратимы, у гетеротрофов сформировались особые ферментативные реакции, разрешающие обходить необратимые реакции катаболического пути.
При расщеплении бактериями-гетеротрофами полисахаридов образующиеся дисахариды поступают вовнутрь клеток и под влиянием мальтозы, сахарозы, лактозы подвергаются распаду и гидролизу на моносахара, каковые после этого сбраживаются или включаются в реакции взаимопревращения сахаров.
Липидный обмен. Исходными материалами для образования липидов у бактерий могут служить как экзогенные липиды, так и амфиболиты межуточного обмена. Экзогенные липиды подвергаются действию бактериальных липаз и других липолитических ферментов. Многие виды бактерий усваивают глицерин, что является источником энергии и пластического материала. Эндогенными источниками для синтеза липидов смогут быть ацетилкоэнзим А, пропионил-АПБ, малонил-АПБ (АПБ – ацетилпереносящий белок), фосфодиоксиацетон и др.
Исходным субстратом для синтеза жирных кислот с чётным числом углеродных атомов помогает ацетилкоэнзим А, для жирных кислот с нечётным числом углеродных атомов – пропионил-АПБ и малонил-АПБ. Образование двойных связей в молекуле кислоты у аэробных прокариот происходит при участии фермента и молекулярного кислорода десатуразы. У анаэробных прокариот двойные связи вводятся на ранних этапах синтеза в следствии реакции дегидратации. Исходным субстратом для синтеза фосфолипидов помогает фосфодиоксиацетон (промежуточное соединение гликолитического пути), восстановление которого ведет к образованию 3-фосфороглицерина. К последнему после этого присоединяются 2 остатка жирных кислот в виде комплекса с АПБ. Продуктом реакции есть фосфатидная кислота, активирование которой посредством ЦТФ и последующее присоединение к фосфатной группе серина, инозита, глицерина либо другого соединения приводят к синтезу соответствующих фосфолипидов.
Ауксотрофные и гипотрофные по жирным кислотам микробы (к примеру, микоплазмы) приобретают их в готовом виде из клеток хозяина либо питательной среды.
Мононуклеотидный обмен. Пуриновые и пиримидиновые мононуклеотиды являются наиболее значимыми компонентами ДНК и РНК. Многие прокариоты способны как применять содержащиеся в питательной среде готовые пуриновые и пиримидиновые основания, их нуклеозиды и нуклеотиды, так и синтезировать их из низкомолекулярных веществ. Бактерии располагают ферментами, катализирующими следующие этапы взаимопревращений экзогенных пуриновых и пиримидиновых производных: азотистое основание – нуклеозид – нуклеотид (моно- – ди- – трифосфат).
Синтез пуриновых и пиримидиновых мононуклеотидов de novo осуществляется свободными дорогами. При синтезе пуриновых нуклеотидов в следствии последовательных ферментативных реакций образуется инозиновая кислота, из которой путём химических модификаций пуринового кольца синтезируются адениловая (АМФ) и гуаниловая (ГМФ) кислоты. Синтез пиримидиновых нуклеотидов начинается с образования оротидиловой кислоты, декарбоксилирование которой даёт уридиловую кислоту (УМФ). Из последней образуется УТФ, ацилирование которого ведет к происхождению ЦТФ.
Дезоксирибонуклеотиды образуются в следствии восстановления соответствующих рибонуклеотидов на уровне дифосфатов либо трифосфатов. Синтез своеобразного для ДНК нуклеотида – тимидиловой кислоты происходит путём ферментативного метилирования дезоксиуридиловой кислоты.
Ионный обмен. Минеральные соединения – ионы, NH3+, К+, Mg2+, Fe2+, SO42-, PO43- и другие бактерии приобретают из экологии как в свободном, так и в связанном с другими органическими веществами состоянии. анионы и Катионы транспортируются в бактериальную клетку разными методами, обрисованными в § 3. На скорость проникновения ионов в бактериальную клетку воздействуют рН среды и физиологическая активность самих микроорганизмов.
Б) Дыхание бактерий (энергетический метаболизм).
Все процессы жизнедеятельности энергозависимы, исходя из этого добывание энергии есть очень важной стороной метаболизма прокариот. Они приобретают энергию при анаэробном и аэробном дыхании.
Дыхание, либо биологическое окисление – это катаболический процесс переноса электронов от вещества-донора на вещество-акцептор, сопровождающийся накоплением энергии в макроэргических соединениях. Дыхание осуществляется в ходе катаболических реакций, из-за которых сложные органические вещества, расщепляясь, отдают энергию и преобразовываются в простые соединения. Аккумулированная в макроэргических веществах (АТФ, ГТФ, УТФ и др.) энергия употребляется в анаболических реакциях.
По методу дыхания микробы подразделяются на облигатные (строгие) аэробы, облигатные и факультативные анаэробы .
Облигатные аэробы нуждаются в свободном кислороде. Донорами электронов у патогенных для человека аэробов-хемоорганотрофов являются органические соединения (углеводы, жиры, белки), акцептором электронов – молекулярный кислород. Запасание энергии в виде АТФ у аэробов-хемоорганотрофов происходит при окислительном фосфорилировании доноров электронов. Аэробы владеют цитохромами (участвуют в переносе электронов), и ферментами (каталаза, супероксиддисмутаза, пероксидаза), инактивирующими токсические кислородные радикалы, образующиеся при дыхании. Супероксиддисмутаза инактивирует самый токсичный метаболит – супероксидрадикал в Н2О2. Фермент каталаза превращает Н2О2 в Н2О и О2.
Особенную группу аэробов составляют микроаэрофильные бактерии, каковые не смотря на то, что и нуждаются в кислороде чтобы получить энергию, лучше растут при повышенном содержании СО2, к примеру, бактерии родов Campylobacter и Helicobacter.
Облигатные анаэробы не нуждаются в свободном кислороде, наоборот, кроме того в малых количествах кислород оказывает на них токсическое воздействие. Донорами электронов у патогенных для человека анаэробов-хемоорганотрофов помогают разные органические соединения (в основном углеводы). Акцептором электронов у анаэробов-хемоорганотрофов являются органические кислородсодержащие соединения – кислоты либо кетоны, другими словами акцептор электрона — связанный с органическим фрагментом кислород. Запасание энергии у этих прокариот происходит при субстратном фосфорилировании. Облигатные анаэробы, в большинстве случаев, не имеют ферментов и цитохромов, инактивирующих кислородные радикалы (каталазо- и супероксидисмутазоотрицательны).
У непатогенных для человека анаэробов хемолитотрофов акцептором электронов являются неорганические кислородсодержащие соединения – нитраты, соли серной кислоты, карбонаты.
Особенную группу анаэробов составляют аэротолерантные бактерии, каковые способны расти в присутствии атмосферного кислорода, но не применяют его в качестве акцептора электронов (к примеру, молочнокислые бактерии). Аэротолерантные прокариоты каталазо- и супероксиддисмутазопозитивны.
Факультативные анаэробы способны существовать как в кислородной, так и в бескислородной средах. Донорами электронов у них являются органические вещества; акцепторами электронов, в зависимости от условий среды – молекулярный либо связанный в органических и неорганических соединениях кислород. Энергия факультативными анаэробами может аккумулироваться как при окислительном, так и при субстратном фосфорилировании. Как и аэробы, эта несколько бактерий имеет ферменты и цитохромы антиоксидантной защиты.
Главным субстратом чтобы получить энергию являются углеводы, каковые у различных по типу дыхания хемогетеротрофных прокариот смогут катаболизироваться до ацетилкоэнзима А («активированная уксусная кислота»). В качестве энергетических субстратов смогут выступать белки и липиды, потому, что ацетилкоэнзим И есть одним из промежуточных продуктов их метаболизма (схема 2).
Катаболизм углеводов у хемоорганотрофных прокариот включает: (а) анаэробные процессы – гликолиз, пентозофосфатный путь и кетодезоксифосфоглюконатный путь; (б) аэробный процесс – цикл трикарбоновых кислот (цикл Кребса). Анаэробные процессы имеют место у всех прокариот, в то время как аэробный процесс характерен лишь для факультативных анаэробов и облигатных аэробов. В базе получения энергии анаэробными дорогами лежит субстратное фосфорилирование, в базе аэробного процесса – окислительное фосфорилирование.
Определение понятий.
Стерилизация, дезинфекция и антисептика являются неотъемлемыми частями современной медицинской и в особенности хирургической практики. Познание практического применения и принципов этих способов нужно, потому, что многие возможно патогенные микробы способны оставаться жизнеспособными вне макроорганизма в течение долгого времени, проявлять высокую устойчивость к действию физических и химических дезинфектантов и довольно легко передаваться от одного человека к второму.
Антисептика — уничтожение либо предотвращение роста патогенных либо условно-патогенных микроорганизмов химическими способами. Данный термин в большинстве случаев применяют для обозначения наружного нанесения химического препарата на живые ткани.
Антисептик — вещество, которое угнетает рост либо разрушает микроб (без действия на споры бактерий). Термин есть своеобразным для обозначения веществ, каковые употребляются для местного действия на живые ткани.
Асептика свидетельствует отсутствие сепсиса, но по большому счету данный термин применяют чтобы выделить отсутствие любых живых организмов. Асептические способы означают любую процедуру, предназначенную для элиминации живых предотвращения и организмов повторной контаминации ними. Современные хирургические и микробиологические способы основаны на асептических процедурах.
Биоцид — вещество, которое убивает все живые микробы, как патогенные, так и непатогенные, включая споры.
Биостат — агент, что предотвращает рост микроорганизмов, но необязательно убивает их.
Деконтаминация — удаление микроорганизмов без количественного определения. Данный термин есть относительным; окончательное удаление микробов возможно осуществлено стерилизацией либо дезинфекцией.
Дезинфекция — процесс, что сокращает количество или полностью уничтожает все патогенные микробы, не считая спор.
Гермицид — вещество, которое разрушает микробы, в особенности патогенные. Гермицид не разрушает споры.
Санация — способ, благодаря которому микробная контаминация значительно уменьшается до “надёжного” уровня. Данный способ ранее применяли для “очищения” неживых объектов.
Стерилизация — применение физических факторов и (либо) веществ для полного уничтожения либо разрушения всех форм микробной судьбе.
Стерилизация.
Стерилизацию определяют как разрушение либо удаление (методом фильтрации) всех микроорганизмов и их спор. Стерилизацию в большинстве случаев выполняют посредством тепла. Стерилизация, будучи одной из повседневных процедур в работе микробиологической лаборатории, есть нужным способом, снабжающим такую обработку, при которой культуры, оборудование, среды и посуда содействуют росту лишь нужных микроорганизмов, в то время как другие микробы разрушаются. Различают такие виды стерилизации: прокаливание в пламени горелки, кипячение, воздействие текучим паром, паром под давлением в автоклаве, сухим жаром, пастеризация, тиндализация, химическая, холодная (механическая) стерилизация.
Выбор способов стерилизации.
При выборе способов стерилизации необходимо учитывать следующие требования:
1. Активность: антибактериальная, спороцидная, туберкулоцидная, фунгицидная и вирусоцидная.
2. Скорость процедуры: стерилизация обязана проводиться максимально скоро.
3. Проницаемость: вещества-стерилизаторы должны попадать через упаковку и к внутренним частям инструментария.
4. Совместимость: не должны появляться трансформации структуры либо функции материалов, каковые стерилизуют пара раз.
5. Нетоксичность: не должно появляться угрозы для состояния и здоровья человека экологии.
6. Устойчивость органического материала: эффективность стерилизации не должна понижаться в присутствия органического материала.
7. Приспособляемость: возможность применять для громадных и малых количеств стерилизуемого материала.
8. Контроль в течение времени: цикл обработки обязан легко и совершенно верно контролироваться.
9. Цена: разумная цена оснащения, эксплуатации и установки.
 Физические стерилизаторы
Физические стерилизаторы
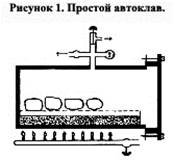
Мокрое тепло, которое образуется в ходе парового автоклавирования, есть главным стерилизующим агентом, применяемым в лабораториях клинической микробиологии. Автоклавы применяют для стерилизации питательных сред, обработки и жароустойчивых материалов инфицированных отходов. Паровой стерилизатор, либо автоклав, представляет собой изолированную камеру под давлением, которая применяет насыщенный пар для больших температур (рис. 1). Воздушное пространство удаляют из камеры замещением по массе либо созданием вакуума. Чаще всего применяют автоклавы с замещением по массе. Более лёгкий пар запускают в камеру для вытеснения более тяжёлого воздуха. Краткосрочная обработка паром под давлением может стереть с лица земли бактериальные споры. Для рутинной стерилизации питательных других материалов и сред время экспозиции образовывает 15 мин. при 121ºС и давление — 1,5 кг на 1 квадратный сантиметр. Для инфекционных отходов время экспозиции возрастает до 30-60 мин.. Дополнительно к верно выбранным времени и температуре, крайне важным при стерилизации есть прямой контакт с паром. При обработке инфекционного материала направляться обеспечить большое проникновение пара в отходы. Таковой материал нужно обрабатывать при температуре 132ºС. Не подлежат автоклавированию антинеопластические препараты, токсичные радиоизотопы и химические вещества, каковые смогут не разрушиться, и нестабильные химикаты, потому, что они под действием тепла смогут испариться и распространиться по камере.
 Стерилизация сухим жаром употребляется для материалов, каковые нереально стерилизовать паром в связи с возможностью повреждения либо в связи с непроницаемостью материала для пара. Сухой жар менее действен, чем мокрое тепло, и требует болеего времени экспозиции и более больших температур. Стерилизацию сухим жаром в большинстве случаев выполняют в сухожаровом шкафу (рис. 2). Механизм стерилизации посредством сухого жара есть окислительным процессом. Примерами материалов, для которых применяют стерилизацию сухим жаром, являются масла, порошки, стеклянная посуда и острые инструменты. Сухой жар либо термическую инактивацию-стерилизацию применяют как другие способы обработки инфекционных отходов.
Стерилизация сухим жаром употребляется для материалов, каковые нереально стерилизовать паром в связи с возможностью повреждения либо в связи с непроницаемостью материала для пара. Сухой жар менее действен, чем мокрое тепло, и требует болеего времени экспозиции и более больших температур. Стерилизацию сухим жаром в большинстве случаев выполняют в сухожаровом шкафу (рис. 2). Механизм стерилизации посредством сухого жара есть окислительным процессом. Примерами материалов, для которых применяют стерилизацию сухим жаром, являются масла, порошки, стеклянная посуда и острые инструменты. Сухой жар либо термическую инактивацию-стерилизацию применяют как другие способы обработки инфекционных отходов.
Пастеризация разрушает патогенные микробы путём стремительного нагревания вещества до 71,1ºС в течении 15 с, что сопровождается последующим стремительным охлаждением. Пастеризация не есть стерилизацией, потому, что не все микробы чувствительны к ней. Данный способ элиминировал пищевой путь передачи таких болезней, как туберкулез пищеварительного тракта и Q-лихорадка.
Тиндализация — это способ стерилизации прерывистым нагреванием, что может употребляться для уничтожения всех бактерий в растворах. Потому, что растущие бактерии легко гибнут при краткосрочном кипячении (5 раз в течение 1 часа по 5 мин.), всё, что нужно сделать, это разрешить раствору постоять в течении определенного времени, перед тем как тепло нарушит созревание спор с значительной утратой их устойчивости к теплу.
Фильтрация — это процесс, что применяют для микроскопических частей и удаления микробов из растворов, воздуха и других газов. Чаще всего стерилизацию методом фильтрации в лаборатории применяют для обработки диагностических препаратов, питательных сред, тканевых культуральных сред, сывороток, растворов, каковые содержат компоненты сыворотки. Вторым общепринятым применением фильтрации есть стерилизация воздуха и газов. Пластиковые либо бумажные мембранные фильтры, каковые различают по диаметру пор (приблизительно от 12 до 0,22 ?м) и применяют для механического разделения, помогают и для сбора микробов из жидкостей для микроскопического изучения либо культивирования прямо на фильтре, в то время, когда его помещают на поверхность, пропитанную питательной средой.
Ультрафиолетовое облучение есть видом электромагнитной волновой радиации, которая действует на клеточную нуклеиновую кислоту. Микробы высокочувствительны к действию ультрафиолетовых лучей с длиной волны 254 нм. Ультрафиолет самый обширно применяют для уничтожения микроорганизмов, находящихся в воздухе либо на каких-либо поверхностях. Вторым применением есть холодная стерилизация определенных химикатов и пластика для фармацевтических целей, стерилизация сыворотки для клеточных культур и дезинфекция воды. Значительным недочётом ультрафиолетового облучения в качестве стерилизатора есть его неспособность к проникновению вовнутрь материалов.
Ионизирующее излучение в электромагнитном спектре летально действует на микробы. Данный спектр включает микроволны, ?-лучи, рентгеновские лучи и поток электронов. Летальный эффект от ионизирующего излучения появляется благодаря прямого действия на молекулу-мишень, в следствии чего энергия переносится в молекулу; и благодаря косвенного действия — диффузии радикалов.
Ультразвуковая энергия с низкой частотой инактивирует микробы в водных растворах. Физический эффект обработки ультразвуком появляется благодаря кавитации. другие приборы и Ультразвуковые очистители довольно часто применяют для очистки инструментов, но не вычисляют стерилизаторами. Но комбинирование ультразвука с химической обработкой убивает микробы.
Химические стерилизаторы
2 % глютаровый альдегид в качестве жидкого химического стерилизатора ранее обширно использовали для обработки медицинского и хирургического материала, что нереально стерилизовать нагреванием либо облучением. Глютаровый альдегид кроме этого применяют при приготовлении вакцин.
Дезинфекция.
Дезинфекцию возможно проводить химическими способами либо кипячением. Кипячение есть действенным способом дезинфекции инструментария, к примеру, игл и шприцев, в случае, если нет автоклава. Предварительно очищенный медицинский инструментарий направляться кипятить 20 мин.. Химическую дезинфекцию применяют для чувствительного к действию тепла оборудования, которое может повредить высокая температура. Обширно применяют такие химические дезинфектанты, как компонента хлора, этиловый и изопропиловый спирт, четвертичные компоненты аммония и глютаровый альдегид.
Химические дезинфектанты.
Спирт (этиловый и изопропиловый), растворённый в воде до концентрации 60-85 %, весьма действен при дезинфекции. Спирты имеют антибактериальное, фунгицидное и туберкулоцидное воздействие, но не воздействуют на споры. Этиловый спирт имеет более широкий спектр вирусоцидной активности, чем изопропиловый, исходя из этого он более действенно действует на липофильные и гидрофильные вирусы.
Раствор 37 % формальдеида, что именуют формалином, возможно применять в качестве стерилизатора, в то время как его концентрации 3-8 % возможно применять в качестве дезинфектантов.
Фенол в чистом виде не применяют в качестве дезинфектанта в связи с его токсичностью, свойством индуцировать коррозии и развитие опухолей. Дериваты фенола, в которых функциональная несколько (хлор, бром, алкил, бензил, фенил, амил) замещает один из атомов водорода в ароматическом кольце, обширно применяют в качестве дезинфектантов. Подобное замещение сокращает недочёты фенола. Компоненты фенола убивают микробы благодаря инактивации ферментных совокупностей, преципитации белков и нарушению клеточной мембраны и стенки. В большинстве случаев применяют концентрации 2-5 %, более низкая концентрация требует более долгой экспозиции.
Галогены. Лишь йод и хлор применяют для дезинфекции в лабораторной практике. В связи с тем, что хлор есть замечательным окислителем, считают, что он убивает микробы методом окисления. Уверены в том, что йод убивает микробы путём реакции с N-H и S-H группами аминокислот, и с фенольной группой аминокислоты тирозина и углерод-углеродными двойными связями ненасыщенных жирных кислот. Простая обработка включает распыление 2-5 % раствора формальдегида в присутствии пара при температуре 60-80ºС.
Антисептика.
Антисептики возможно найти в микробиологических лабораториях, в первую очередь, в веществах, каковые применяют для мытья рук. В тех случаях, в то время, когда медицинский персонал оказывает неотложную помощь больным с применением веществ, содержащих бактерицидные агенты, это сокращает количество госпитальных зараз. Самый распространёнными химическими соединениями, содержащимися в веществах для мытья рук, являются спирты, хлоргексидина глюконат, йодофоры, хлороксайленол и триклозан.
Классическими способами мусора и обработки отходов являются стерилизация и сжигание паром.
Сжигание есть способом выбора для мусора и обработки отходов. Данный способ делает отходы неинфекционными, и изменяет их размеры и форму. Стерилизация есть действенным способом обработки отходов, но она не изменяет их формы. Стерилизация паром в автоклаве при 121ºС в течение минимум 15 мин. уничтожает все формы микробной судьбе, включая много бактериальных спор. Данный тип полной стерилизации кроме этого возможно совершить с применением сухого жара при температуре 160-170ºС в течении 2-4 часов. Но направляться убедиться, что сухой жар контактирует со стерилизуемым материалом. Исходя из этого бутылки, каковые содержат жидкость, должны быть неплотно закрыты пробками либо ватными тампонами чтобы жар и пар имели возможность обмениваться с воздухом в бутылках. Биологически страшные контейнеры, которые содержат отходы, направляться хорошо завязать. Простерилизованный биологически страшный материал необходимо запечатать в соответствующие контейнеры с этикетками.
Стерилизация паром (в автоклаве). Инфекционный мусор вычисляют деконтаминированным при уменьшении в 6 lg раз количества вегетативных бактерий, грибов, микобактерий и вирусов, содержащих липиды, и в 4 lg раза — бактериальных эндоспор.
Питание бактерий.
Питание. Под едой бактериальной клетки направляться осознавать усвоения и процесс поглощения энергии и пластического материала в следствии преобразовательных реакций. Типы питания прокариот сложны и разнообразны. Они различаются в зависимости от метода поступления питательных веществ вовнутрь бактериальной клетки, азота и источников углерода, метода получения энергии, природы доноров электронов.
Транспорт питательных веществ вовнутрь клетки может осуществляться 3 механизмами: пассивной диффузией, облегчённой активным транспортом и диффузией.
Пассивная диффузия есть неспецифическим энергозависимым процессом, осуществляемым по градиенту концентрации веществ (вещество из среды с большей собственной концентрацией пассивно, в соответствии с законам осмоса, поступает в среду с меньшей концентрацией). Пассивной диффузией вовнутрь бактериальной клетки поступает ограниченное количество веществ, кое-какие ионы, моносахара. Скорость переноса веществ при пассивной диффузии незначительна и зависит от липофильности и размеров транспортирующихся молекул.
Облегчённая диффузия представляет собой энергонезависимый транспорт веществ по градиенту концентрации при помощи ферментов пермеаз. Пермеазы – это своеобразные мембранные белки, содействующие прохождению веществ через цитоплазматическую мембрану. Пермеаза фиксирует на себе молекулу переносимого вещества, вместе с которым пеодолевает цитоплазматическую мембрану, по окончании чего комплекс «вещество – пермеаза» диссоциирует. Освободившаяся пермеаза употребляется с целью проведения вторых молекул. У прокариотов облегчённой диффузией вовнутрь клетки поступает лишь глицерин. Наряду с этим концентрация внутри клетки глицерина соответствует такой вне клетки. Облегчённая диффузия самый характерна для микроорганизмов-эукариот.
Деятельный транспорт – это энергозависимый перенос веществ вовнутрь клетки против градиента концентрации при помощи своеобразных ферментов. Активным транспортом в бактериальную клетку поступает большинство веществ (ионы, углеводы, аминокислоты, липиды и др.). Деятельный транспорт может осуществляться: (1) без химической модификации переносимого вещества; (2) с химической модификацией.